Há muitos anos atrás, na Grécia antiga, um filósofo teve a brilhante ideia de que se ao pegar um objeto, e corta-lo diversas vezes em partes menores, chegaríamos à menor matéria existente, que ele chamou de átomo.
Thomson
Demócrito (460 a.C.) foi o filósofo responsável por defender essa ideia, as coisas eram formadas por minúsculas partículas, ele estava certo, porém, diferente de como ele imaginou, os átomos são divisíveis, neste ponto estava errado, pois acreditou que fossem indivisíveis, e isso foi descoberto por Joseph Thomson (físico inglês, 1856-1940), Thomson anunciou que haviam partículas ainda menores dentro do átomo e que ele era divisível.
O novo modelo atômico que Thomson propôs era: o átomo seria uma esfera carregada positivamente com partículas negativas em sua superfície.
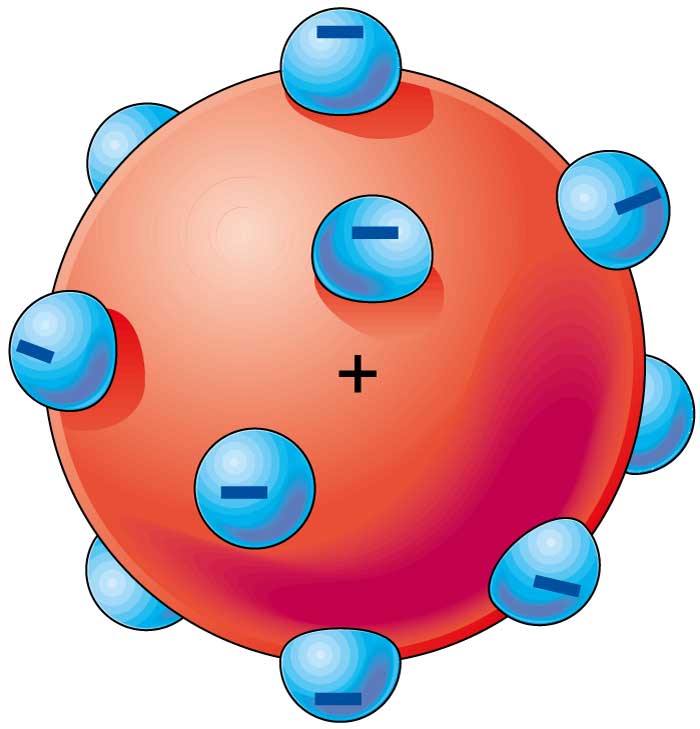
Esse modelo foi chamado de pudim de passas: a esfera positiva seria o pudim e os elétrons, as passas.
Rutherford
No entanto, Ernest Rutherford (físico neozelandês, 1871-1937), ao verificar o comportamento de partículas dirigidas contra uma chapa metálica em experiências posteriores, obteve resultados que contrariavam todas as previsões baseadas no modelo de Thomson. Com essas novas observações Rutherford propôs outro modelo: o átomo seria formado por duas regiões, uma central – o núcleo atômico, extremamente compacta, densa e com carga elétrica positiva – e outra periférica – a eletrosfera, na qual os elétrons estariam circulando ao redor do núcleo, como os planetas em torno do Sol.
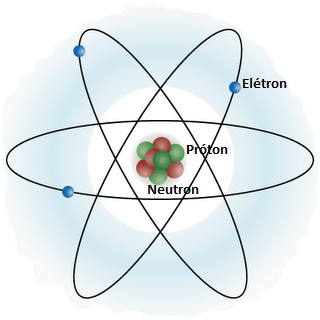
O modelo de Rutherford , no entanto, não era suficiente, a falha desse modelo é mostrada pela teoria do eletromagnetismo. Naquela época já era conhecido o fato de que, se uma carga elétrica fosse submetida a tais condições , ela irradiaria energia, descreveria uma órbita em espiral e cairia no núcleo atômico.
Bohr
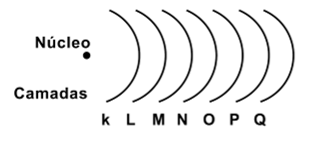
Niels Bohr (físico dinamarquês, 1885 – 1962) aprofundou-se no estudo desse problema e aprimorou o modelo atômico de Rutherford. Bohr propôs que: os elétrons firam ao redor do núcleo em órbitas, denominadas níveis de energia ou camadas eletrônicas; o elétron não perde energia enquanto gira em determinada órbita; em cada órbita, o elétron tem energia específica; o elétron pode saltar de uma órbita para outra.
É como se cada elétron estivesse em um degrau de uma escada. Enquanto permanece no degrau tem sempre a mesma energia. No entanto, para subir um degrau deve ganhar energia. Para descer, tem de devolver a mesma quantidade de energia recebida.
Atualmente
Hoje, sabe-se que os átomos são formados por inúmeras partículas, chamadas subatômicas, como os prótons, elétrons, nêutrons, pósitrons, quarks, neutrinos e mésons, as partículas fundamentais para o átomo, são, no entanto, os prótons, os elétrons e os nêutrons.
Os prótons e os nêutrons estão situados no núcleo atômico; os elétrons ao redor do núcleo, na eletrosfera. Os prótons e elétrons são partículas eletricamente carregadas, o próton sendo carga positiva e o elétron carga negativa. já os nêutrons não possuem carga elétrica.


